Carlos Fernando Mourão e Gutemberg Gomes Alves
Resumo Executivo
Os derivados plaquetários, incluindo o Plasma Rico em Plaquetas (PRP) e a Fibrina Rica em Plaquetas (PRF), emergiram como ferramentas essenciais na medicina regenerativa ao concentrar sinais autólogos que coordenam o reparo tecidual. No entanto, o campo atualmente é caracterizado por significativa heterogeneidade na composição dos produtos e nos desfechos clínicos.
Este documento apresenta as distinções biológicas entre as principais famílias de derivados plaquetários, identifica as variáveis técnicas que dificultam a consolidação de evidências e apresenta estruturas emergentes para padronização.
O principal insight é uma mudança de paradigma na pesquisa regenerativa: sair da pergunta genérica sobre se os derivados plaquetários “funcionam” para uma compreensão precisa de qual preparação, em qual dose e regime, é mais adequada para tecidos e perfis de pacientes específicos. Para isso, é necessária a adesão rigorosa a padrões mínimos de relato e a adoção de métricas de qualidade, como o modelo DEPA (Dose, Eficiência, Pureza, Ativação).
1. Fundamentos Biológicos dos Derivados Plaquetários
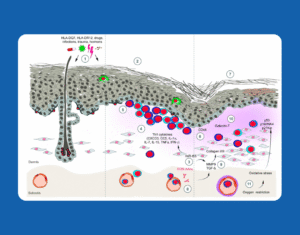
Os derivados plaquetários atuam como reguladores transitórios do microambiente celular. Eles não apenas aumentam a disponibilidade de fatores de crescimento, mas também modulam ativamente interações imune-estromais, migração celular e organização da matriz extracelular.
1.1 Famílias Funcionais e Cinética de Liberação
O desempenho biológico de um derivado é determinado por sua forma física, conteúdo celular e cinética de liberação:
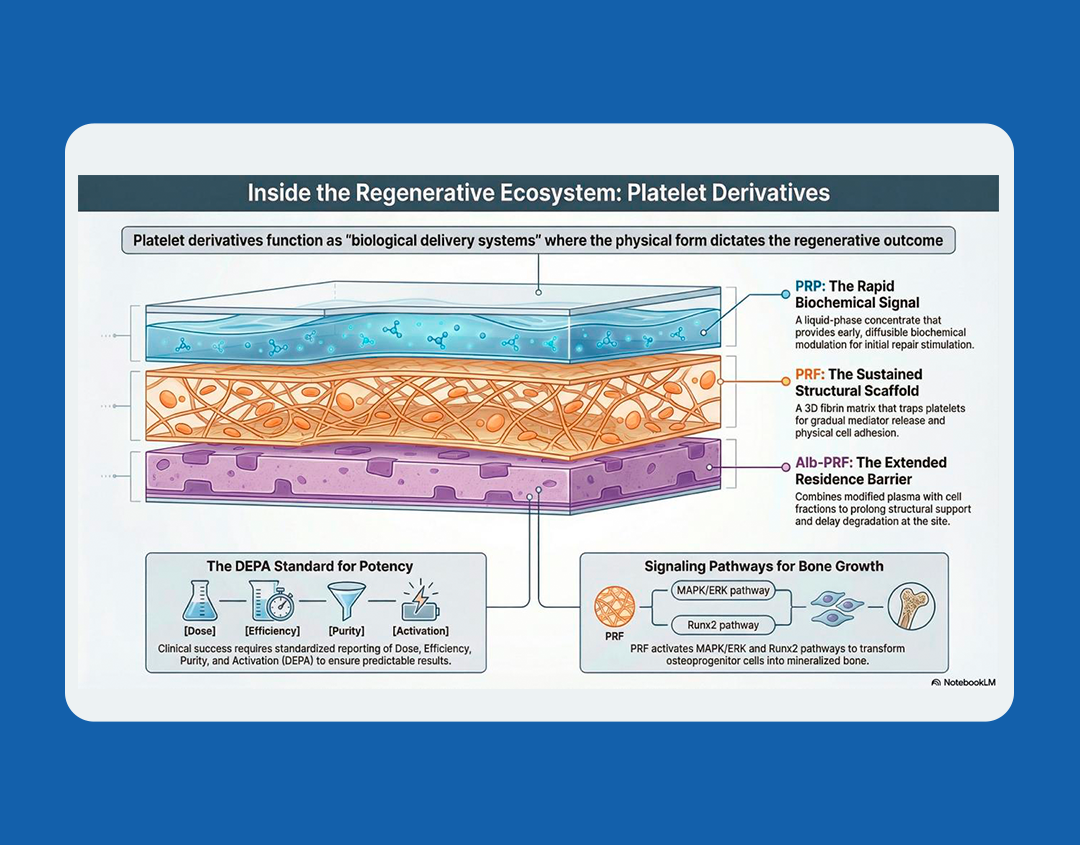
• Plasma Rico em Plaquetas (PRP): um concentrado em fase líquida que favorece difusão rápida e sinalização precoce. Atua principalmente como uma “dose biológica” para modulação bioquímica em tecidos bem vascularizados. Não possui um arcabouço mecânico intrínseco, a menos que seja ativado (por exemplo, com cloreto de cálcio ou trombina) para induzir gelificação.
• Fibrina Rica em Plaquetas (PRF): caracterizada por uma matriz tridimensional de fibrina que retém plaquetas e leucócitos. Essa estrutura permite liberação sustentada de mediadores e fornece um arcabouço temporário para adesão celular e organização tecidual.
• Frações plasmáticas modificadas (ex.: Alb-PRF): obtidas pela combinação de plasma desnaturado (aquecido) com uma fração rica em células. Essas formulações priorizam estabilidade física e maior tempo de permanência no local cirúrgico, estendendo o suporte local além dos limites do PRF convencional.
• Lisado Plaquetário Humano (HPL): produto acelular baseado no conteúdo liberado pela lise das plaquetas. Oferece um “coquetel” de mediadores solúveis em liberação única. Embora não possua liberação sustentada, sua previsibilidade o torna ideal para expansão celular e engenharia de tecidos.
• Vesículas Extracelulares Derivadas de Plaquetas (EVs): uma categoria emergente e ainda exploratória, que pode transmitir sinais bioativos direcionados. Contudo, ainda carece de protocolos padronizados de isolamento e dados robustos de dose-resposta.
1.2 Programação Celular e Vias de Sinalização
Os derivados plaquetários modulam programas celulares definidos, e não atuam como misturas inespecíficas. Por exemplo, em células mineralizantes, o PRF ativa vias específicas (MAPK/ERK e PI3K/AKT) que convergem em reguladores centrais como RUNX2 e Osterix (OSX).
Isso resulta na expressão de genes relacionados à matriz (ALP, COL1, Osteocalcina) e na maturação de osteoblastos em osteócitos.
2. Variáveis Técnicas e Barreiras à Reprodutibilidade
Uma das principais barreiras para a aplicação clínica é o “ecossistema” de preparações frequentemente agrupadas sob os mesmos termos genéricos, apesar de serem biologicamente distintas.
2.1 Impacto da Centrifugação e dos Materiais
Pequenas mudanças técnicas durante a preparação geram grandes diferenças no produto final:
• Parâmetros de centrifugação: duração, velocidade e força centrífuga relativa (RCF) determinam a separação das camadas e as propriedades biológicas e mecânicas do concentrado.
• Tipos de tubos: para PRP, são necessários tubos com anticoagulantes (ex.: citrato de sódio). Para PRF sólido, utilizam-se tubos sem anticoagulantes (geralmente de vidro ou revestidos com sílica) para promover coagulação rápida.
• Tempo de manipulação: no PRF líquido (i-PRF), o intervalo entre coleta, centrifugação e aplicação é crítico; variações de poucos minutos podem determinar se o material permanece injetável ou se polimeriza em coágulo.
2.2 Variabilidade do Doador e Contexto Biológico
Mesmo com protocolos idênticos, variáveis individuais impactam os resultados:
• Características do paciente: idade, comorbidades e níveis de inflamação sistêmica alteram o perfil celular e molecular do derivado.
• Conteúdo leucocitário: a inclusão ou exclusão de leucócitos (frequentemente omitida em estudos) influencia significativamente os efeitos imunomoduladores e a polarização de macrófagos.
3. Padronização e Métricas de Qualidade
Para elevar os derivados plaquetários a um padrão moderno na medicina regenerativa, é essencial adotar métricas objetivas de caracterização e relato.
3.1 Estrutura DEPA
O sistema DEPA substitui descrições qualitativas (“PRP rico” ou “forte”) por uma lógica de produção mensurável:
• Dose: número total de plaquetas administradas (Concentração × Volume)
• Eficiência: taxa de recuperação de plaquetas em relação ao sangue inicial
• Pureza: composição relativa de plaquetas, leucócitos e eritrócitos
• Ativação: registro de se e como o produto foi ativado (ex.: CaCl₂)
3.2 Checklist Mínimo de Relato
A tabela abaixo resume os parâmetros essenciais para permitir comparação entre estudos e replicação clínica:
Coleta
Tipo e concentração do anticoagulante, volume total de sangue, material do tubo (vidro/plástico/aditivos)
Processamento
RCF (×g), tempo de centrifugação, número de ciclos, tipo de rotor (ângulo fixo ou basculante)
Manipulação
Intervalos entre coleta, centrifugação e aplicação
Produto final
Família do produto (PRP, PRF, Alb-PRF, HPL), volume/dimensões e método de ativação
Composição
Contagem de plaquetas, leucócitos e eritrócitos (validadas por hemocitometria automatizada)
Aplicação
Forma física (líquido/gel/membrana), dose administrada e método/local de aplicação
4. Direções Futuras: Desenho Racional de Estudos
As tendências atuais enfatizam alinhar o tipo de derivado às necessidades biológicas do tecido-alvo:
• Necessidade de arcabouço: em aplicações que exigem efeito prolongado (ex.: harmonização facial), há migração para formulações como Alb-PRF, que ampliam o tempo de reabsorção.
• Seleção de desfechos: os desfechos clínicos devem ser compatíveis com o tempo de permanência do produto — PRP para respostas precoces, PRF e derivados modificados para efeitos mais sustentados.
• Evitar a “inflação de variantes”: embora existam múltiplas variações de protocolos PRF, há pouca evidência de que pequenas modificações gerem diferenças clínicas relevantes. O foco deve ser em estudos bem controlados, não na criação de novos rótulos.
Conclusão
Os derivados plaquetários ocupam papel central na medicina regenerativa por combinarem sinalização biológica com viabilidade prática.
No entanto, sua aplicação clínica depende da transição de uma terminologia genérica para produtos bem definidos, com qualidade mensurável e desfechos biologicamente plausíveis.
A padronização e o relato consistente das variáveis de preparo são o primeiro passo essencial para a maturidade desse campo.
LEIA MAIS EM: https://www.frontiersin.org/journals/cell-and-developmental-biology/articles/10.3389/fcell.2026.1770953/full