Stewart W. Ross, Josephine Malcolm, Joanneke Maitz, Zhe Li, Yiwei Wang, Andrea C. Issler-Fisher
Resumo
O resurfacing fracionado ablativo é clinicamente um tratamento eficiente para o manejo de cicatrizes de queimaduras. O objetivo deste estudo piloto foi investigar os mecanismos ainda pouco compreendidos subjacentes à terapia com laser de CO2 fracionado ablativo (AFL-CO2) em relação aos biomarcadores S100 e 11β-hidroxiesteroide desidrogenase tipo 1 (11β-HSD1).
A proteína S100 cora células de Langerhans e células neuronais, podendo representar potencialmente o prurido experimentado. A 11β-HSD1 catalisa a interconversão de cortisol e cortisona nas células, promovendo o remodelamento tecidual.
Foi realizada análise imuno-histoquímica da expressão das proteínas S100 e 11β-HSD1 na derme e na epiderme da pele em pele normal e em pele antes e após a terapia com AFL-CO2. Dados referentes aos parâmetros de desfecho foram coletados simultaneamente com as biópsias de pele.
Treze pacientes foram tratados com terapia AFL-CO2. As células de Langerhans diminuíram em 39% após o segundo tratamento. As células neuronais apresentavam superexpressão antes do tratamento no tecido cicatricial em 91%, porém os níveis retornaram a valores semelhantes aos da pele normal.
A expressão de 11β-HSD1 em queratinócitos foi significativamente maior após o tratamento com laser em comparação com antes do tratamento no tecido cicatricial (p < 0,01). Nenhuma correlação clara foi encontrada no número de fibroblastos dérmicos ao longo do curso do tratamento.
Embora o papel dos mecanismos investigados e sua associação com os desfechos clínicos não possa ser afirmado de forma conclusiva, este estudo piloto demonstra tendências promissoras que incentivam investigações adicionais sobre essa relação.
Introdução
A formação de cicatrizes no tecido cutâneo humano é resultado de um processo complexo de cicatrização de feridas que envolve diversas vias moleculares e de sinalização.
As queimaduras apresentam elevada propensão ao desenvolvimento de cicatrizes hipertróficas devido à natureza inflamatória da lesão e ao tempo prolongado de cicatrização.
A cicatriz hipertrófica caracteriza-se por ser firme, elevada, rígida e irregular, podendo resultar em contraturas que limitam a amplitude de movimento das articulações.
Além disso, sintomas associados à cicatriz, como prurido, dor neuropática e o impacto psicológico da lesão, podem ter efeito prejudicial sobre a saúde geral e a qualidade de vida de sobreviventes de queimaduras.
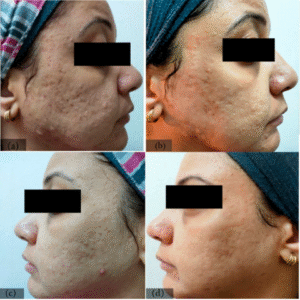
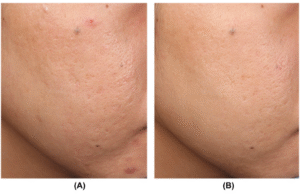
Os efeitos positivos observados em diversos parâmetros de avaliação de cicatrizes — incluindo características clínicas da cicatriz, dor neuropática, prurido e qualidade de vida específica para queimaduras — levaram à incorporação da terapia com laser de CO2 fracionado ablativo (AFL-CO2) no tratamento rotineiro de cicatrizes de queimaduras em muitas unidades especializadas.
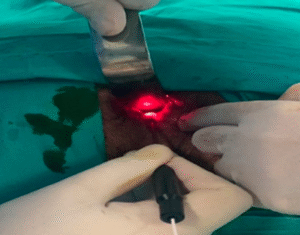
A terapia a laser fracionado ablativo aplica energia por meio de microfeixes pixelizados. A alta energia do laser induz temperaturas superiores a 100 °C nos tecidos, produzindo colunas de tecido cicatricial vaporizado alternadas com colunas de tecido saudável. Esse processo permite que o colágeno da pele ou da cicatriz seja remodelado por meio da resposta de cicatrização da ferida.
Glicocorticoides são frequentemente utilizados como tratamento tópico ou injeções intralesionais após a terapia de cicatriz com AFL-CO2 para auxiliar na redução da inflamação.
As pesquisas atuais sobre terapia a laser e cicatrizes de queimaduras concentram-se principalmente na melhoria das características da cicatriz hipertrófica, como firmeza, elevação e tamanho da cicatriz, ou em marcadores associados, incluindo CD14 e TLR4.
No entanto, até onde sabemos, não existem dados disponíveis investigando marcadores potenciais associados à melhora de sintomas relacionados à cicatriz, como prurido e dor após resurfacing a laser.
Os mecanismos bioquímicos subjacentes, especialmente aqueles relacionados a desfechos específicos do paciente, ainda não são completamente compreendidos, particularmente no que se refere à dor e ao prurido associados a cicatrizes de queimadura.
Com base em evidências anteriores que demonstram redução significativa do prurido e da dor neuropática após tratamento com AFL-CO2, este estudo piloto foi realizado para investigar possíveis mecanismos moleculares associados a esses efeitos clínicos.
Neste projeto piloto, duas proteínas foram investigadas antes e após o tratamento a laser:
- a família de proteínas S100
- a isoforma 11β-HSD tipo 1 (11β-HSD1)
As proteínas S100 são uma família de pequenas proteínas ligadoras de cálcio presentes em uma grande variedade de tecidos.
Na pele humana, a proteína S100 está presente principalmente em células apresentadoras de antígenos e células mielinizadas, além de diversos tumores.
O anticorpo escolhido para este experimento foi um anticorpo para S100 beta.
Na epiderme da pele, o anticorpo S100 liga-se às células de Langerhans e aos melanócitos.
Na derme da pele, S100 liga-se a células neuronais mielinizadas, como as terminações de Ruffini e os discos de Merkel, além de células axonais presentes na rede neural cutânea.
As células de Langerhans são células dendríticas diferenciadas que respondem à irritação da pele liberando citocinas, o que é percebido como sensação dolorosa na área da cicatriz.
Além disso, foi demonstrado que as células de Langerhans estão correlacionadas à formação de cicatrizes hipertróficas.
O objetivo da utilização do marcador S100 foi investigar se a terapia com AFL-CO2 possui efeito sobre o número de células de Langerhans dentro da cicatriz e comparar os resultados com os desfechos clínicos de melhora da dor e do prurido.
A enzima 11β-HSD1 é uma das duas isoformas de uma enzima localizada no retículo endoplasmático das células em diversos tecidos e possui a função de converter cortisona em cortisol ou corticosterona, fornecendo aos tecidos circundantes um suprimento endógeno de cortisol.
Estudos envolvendo 11β-HSD1 na pele são relativamente recentes.
Na pele, a 11β-HSD1 está presente em fibroblastos dérmicos, melanócitos e queratinócitos.
O efeito dessa enzima nas células circundantes está relacionado principalmente ao cortisol produzido, que possui propriedades anti-inflamatórias e influencia a proliferação dos queratinócitos.
Glicocorticoides como o cortisol são utilizados como tratamentos tópicos para queimaduras, e por isso hipotetiza-se que a liberação de cortisol endógeno possa auxiliar no processo de cicatrização.
A ativação local da 11β-HSD1 demonstrou efeitos variados na pele.
O aumento de glicocorticoides na pele reduz a proliferação de queratinócitos e fibroblastos, o que tem efeito positivo no desfecho clínico de cicatrizes hipertróficas.
Os glicocorticoides também reduzem a inflamação dentro e ao redor da cicatriz, promovendo cicatrização mais eficiente.
Além disso, a integridade da pele resultante da presença de glicocorticoides beneficia o processo de cicatrização, pois promove a ruptura dos feixes de colágeno compactados, permitindo que a substância fundamental infiltre-se no tecido.
Dessa forma, a expressão de S100 e 11β-HSD1 na pele foi investigada em relação ao tratamento com laser para elucidar melhor os mecanismos envolvidos na cicatrização de cicatrizes tratadas com terapia a laser.
Com base na experiência clínica com a tecnologia AFL-CO2, esperava-se observar diminuição da expressão de S100 e aumento da expressão de 11β-HSD1 na pele, indicando que a terapia melhora tanto a cicatrização da cicatriz quanto os desfechos subjetivos relatados pelos pacientes.
Trechos de seção
Coleta de dados
Todos os dados dos pacientes e biópsias de tecido cutâneo foram coletados na Unidade de Queimados do Concord Repatriation General Hospital (CRGH), em Sydney, Austrália, um centro estadual de referência para pacientes queimados e hospital de ensino da Universidade de Sydney, seguindo um protocolo bem estabelecido e aprovado pelo comitê de ética.
Os critérios de elegibilidade incluíram pacientes com cicatrizes hipertróficas após queimaduras capazes de fornecer consentimento informado.
Resultados imuno-histoquímicos
Nenhuma diferença significativa foi encontrada na população de células de Langerhans na epiderme ao longo do tratamento com AFL-CO2.
Antes do tratamento, foi quantificada média de 5 células de Langerhans por 100.000 µm² no tecido cicatricial, valor semelhante às 7 células por 100.000 µm² encontradas em tecido normal saudável.
Após o tratamento, houve aumento para 7 células por 100.000 µm².
O segundo tratamento com AFL-CO2 resultou em redução de 39% das células de Langerhans em comparação ao primeiro tratamento.
Análise imuno-histoquímica
O presente estudo indica que os marcadores escolhidos revelam um processo mais complexo subjacente à terapia AFL-CO2 que não pode ser compreendido apenas investigando os efeitos mediados por 11β-HSD1 ou S100, uma vez que poucas alterações estatisticamente significativas foram observadas na expressão dessas moléculas durante o tratamento.
A alteração no número de células de Langerhans foi inconclusiva quanto à relação com a terapia a laser.
Conclusão
Em conclusão, não há ligação definitiva entre a terapia a laser e os marcadores S100 e 11β-HSD1 e seus efeitos sobre as cicatrizes.
A expressão de S100 na pele não pode ser diretamente associada à ação da terapia AFL-CO2, e não se pode concluir que a degradação do colágeno nas cicatrizes seja atribuída à produção endógena de cortisol, apesar dos resultados promissores da expressão de 11β-HSD1 na epiderme.
Este estudo piloto indica a necessidade de investigações adicionais para compreender melhor os mecanismos envolvidos na cicatrização de cicatrizes tratadas com terapia a laser.
Leia mais em: https://doi.org/10.1016/j.burns.2022.12.017